Matemática
Para entender o conceito básico da geometria molecular, podemos partir de uma analogia bastante simples, com algumas observações do mundo macroscópico. Sempre que tentamos agrupar aleatoriamente objetos materiais sólidos de determinado formato, notamos que há uma relação direta entre o formato do objeto e o formato final do agrupamento.
Assim, quando jogamos esferas em uma caixa, por exemplo, elas tendem a deslizar umas sobre as outras e assumir uma configuração final organizada, adequada ao formato da caixa.
Se na mesma caixa jogarmos palitos de fósforo, teremos no final um empilhamento caótico, possivelmente uma pirâmide deformada, sem contornos definidos. Com as moléculas acontece coisa semelhante, só que acrescida de um fator que falta às esferas e fósforos do exemplo.
Elétrons e zonas de repulsão
Quando dois ou mais átomos se unem para formar uma molécula, suas eletrosferas entram em contato e o formato de seus orbitais (esféricos ou elípticos) influenciará o formato final da ligação. Só que, neste caso, o formato não é o único fator de influência, já que, ao contrário de nossas esferas e fósforos, as eletrosferas são compostas de elétrons, partículas eletricamente carregadas.
Como os elétrons têm carga negativa, se repelem entre si. Esta repulsão eletrostática influencia de modo definitivo a geometria molecular, ou seja, o formato do agrupamento de átomos que constitui a molécula. Este fator de influência das cargas elétricas negativas dos elétrons na disposição geométrica da molécula é chamado de zonas de repulsão.
Uma zona de repulsão se cria em torno de uma ligação molecular, ou seja, nas vizinhanças dos elétrons compartilhados pelos átomos que formam a molécula.
O efeito das zonas de repulsão tende a formar três disposições geométricas básicas em um molécula apolar (aquela na qual os elétrons não se concentram em pólos): a linear, a triangular plana e a tetraédrica, conforme as três figuras a seguir:
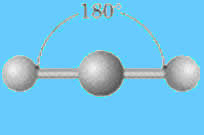
Disposição geométrica linear. Os átomos se posicionam em linha.
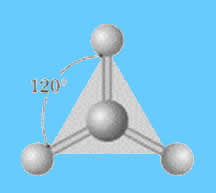
Disposição geométrica triangular plana. Os átomos formam um triângulo eqüilátero.
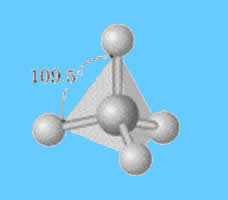
Disposição geométrica tetraédrica. Formato de tetraedro (pirâmide triangular).
Para se determinar a disposição geométrica de uma molécula, basta seguir duas regras simples:
1) Escrever a fórmula estrutural;
2) Identificar o número de ligações atômicas, que é o mesmo número de zonas de repulsão;
Se a molécula tiver até duas zonas de repulsão, a geometria será linear. Se tiver três, será triangular plana e se tiver quatro será tetraédrica.
Vejamos alguns exemplos:
1) Molécula de Dióxido de Carbono (CO2)
Fórmula estrutural:
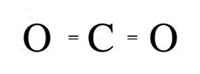
Note que o átomo de carbono estabelece duas duplas ligações, uma dupla ligação com cada átomo de oxigênio. A molécula de CO2 também pode ser representada conforme abaixo:
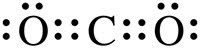
Se a molécula possui duas duplas ligações, possui também duas zonas de repulsão, que tendem a se afastar uma da outra, fazendo com que a molécula assuma a disposição geométrica linear, conforme a seguinte figura:

Representação esquemática da molécula de dióxido de carbono, que apresenta geometria linear.
2) Molécula de Trifluoreto de Boro (BF3)
Fórmula estrutural:
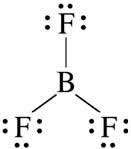
Como vemos, o átomo de boro forma três ligações simples, uma com cada átomo de flúor. Assim temos três zonas de repulsão e a geometria molecular é triangular plana, conforme a figura:
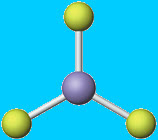
Representação esquemática da geometria triangular plana do Trifluoreto de Boro (BF3)
3): Molécula de Metano (CH4)
Fórmula estrutural:
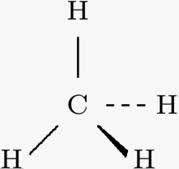
O carbono estabelece quatro ligações simples, uma com cada átomo de hidrogênio, logo temos quatro zonas de repulsão e a geometria molecular é tetraédrica, conforme figura abaixo:
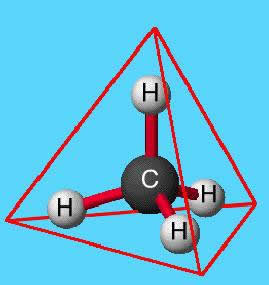
Representação esquemática da molécula de Metano, de geometria tetraédrica.
A geometria é uma ferramenta preciosa para entendermos o universo. Ela nos ajuda tanto a descrever a grandeza cósmica das órbitas planetárias quanto nos auxilia na visão do inimaginavelmente pequeno das formas das moléculas.
Um excelente lembrete de que as disciplinas do conhecimento podem ser separadas para melhor administração de currículos escolares, mas que todas devem ser integradas na construção individual do conhecimento.
*Carlos Roberto de Lana é professor e engenheiro químico.
- Compostos Orgânicos: Características Gerais
Líria Alves A cetona é um composto orgânicoOs compostos orgânicos em sua maioria são formados pela ligação entre átomos de carbono e hidrogênio. Sendo assim, a atração entre elétrons das moléculas orgânicas é praticamente...
- Lei De Avogadro
Do número de Avogadro, sabemos que há aproximadamente 6,02 x 1023 átomos/mol. Então, em 0,0142 mol temos : (0,0142 mol) x (6,02 x 1023 átomos/mol) = 8,55 x 1021átomos Volume molar de um gás CNTP: temperatura = 0 °C e pressão =1atm. É o volume...
- Substâncias
Uma das maiores confusões que as pessoas fazem na hora de classificar as substâncias reside nos quesitos de substância simples e substância pura. Para que isso fique claro é fundamental que entendamos bem algumas coisas antes de chegarmos a essa...
- Química Geral
I - PROPRIEDADES DAS SUBSTÂNCIAS 1) Substância Iônica: Possuem elevados ponto de fusão (PF) e ponto de ebulição (PE);São solúveis em solventes polares;Conduzem a corrente elétrica quando fundidos (fase líquida) ou em solução aquosa, situações...
- A Ligação Covalente Da Quimica
Professor de Matemática e Biologia Antônio Carlos Carneiro BarrosoColégio Estadual Dinah Gonçalvesemail [email protected] www.ensinodematemtica.blogspot.com.brwww.accbarrosogestar.blogspot.com.br WWW.profantoniocarneiro.com ...
Matemática
Geometria molecular Distribuição espacial dos átomos em uma molécula
Para entender o conceito básico da geometria molecular, podemos partir de uma analogia bastante simples, com algumas observações do mundo macroscópico. Sempre que tentamos agrupar aleatoriamente objetos materiais sólidos de determinado formato, notamos que há uma relação direta entre o formato do objeto e o formato final do agrupamento.
Assim, quando jogamos esferas em uma caixa, por exemplo, elas tendem a deslizar umas sobre as outras e assumir uma configuração final organizada, adequada ao formato da caixa.
Se na mesma caixa jogarmos palitos de fósforo, teremos no final um empilhamento caótico, possivelmente uma pirâmide deformada, sem contornos definidos. Com as moléculas acontece coisa semelhante, só que acrescida de um fator que falta às esferas e fósforos do exemplo.
Elétrons e zonas de repulsão
Quando dois ou mais átomos se unem para formar uma molécula, suas eletrosferas entram em contato e o formato de seus orbitais (esféricos ou elípticos) influenciará o formato final da ligação. Só que, neste caso, o formato não é o único fator de influência, já que, ao contrário de nossas esferas e fósforos, as eletrosferas são compostas de elétrons, partículas eletricamente carregadas.
Como os elétrons têm carga negativa, se repelem entre si. Esta repulsão eletrostática influencia de modo definitivo a geometria molecular, ou seja, o formato do agrupamento de átomos que constitui a molécula. Este fator de influência das cargas elétricas negativas dos elétrons na disposição geométrica da molécula é chamado de zonas de repulsão.
Uma zona de repulsão se cria em torno de uma ligação molecular, ou seja, nas vizinhanças dos elétrons compartilhados pelos átomos que formam a molécula.
O efeito das zonas de repulsão tende a formar três disposições geométricas básicas em um molécula apolar (aquela na qual os elétrons não se concentram em pólos): a linear, a triangular plana e a tetraédrica, conforme as três figuras a seguir:

Disposição geométrica linear. Os átomos se posicionam em linha.

Disposição geométrica triangular plana. Os átomos formam um triângulo eqüilátero.

Disposição geométrica tetraédrica. Formato de tetraedro (pirâmide triangular).
Para se determinar a disposição geométrica de uma molécula, basta seguir duas regras simples:
1) Escrever a fórmula estrutural;
2) Identificar o número de ligações atômicas, que é o mesmo número de zonas de repulsão;
Se a molécula tiver até duas zonas de repulsão, a geometria será linear. Se tiver três, será triangular plana e se tiver quatro será tetraédrica.
Vejamos alguns exemplos:
1) Molécula de Dióxido de Carbono (CO2)
Fórmula estrutural:
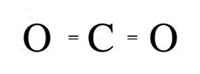
Note que o átomo de carbono estabelece duas duplas ligações, uma dupla ligação com cada átomo de oxigênio. A molécula de CO2 também pode ser representada conforme abaixo:
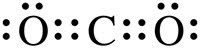
Se a molécula possui duas duplas ligações, possui também duas zonas de repulsão, que tendem a se afastar uma da outra, fazendo com que a molécula assuma a disposição geométrica linear, conforme a seguinte figura:

Representação esquemática da molécula de dióxido de carbono, que apresenta geometria linear.
2) Molécula de Trifluoreto de Boro (BF3)
Fórmula estrutural:

Como vemos, o átomo de boro forma três ligações simples, uma com cada átomo de flúor. Assim temos três zonas de repulsão e a geometria molecular é triangular plana, conforme a figura:

Representação esquemática da geometria triangular plana do Trifluoreto de Boro (BF3)
3): Molécula de Metano (CH4)
Fórmula estrutural:

O carbono estabelece quatro ligações simples, uma com cada átomo de hidrogênio, logo temos quatro zonas de repulsão e a geometria molecular é tetraédrica, conforme figura abaixo:

Representação esquemática da molécula de Metano, de geometria tetraédrica.
A geometria é uma ferramenta preciosa para entendermos o universo. Ela nos ajuda tanto a descrever a grandeza cósmica das órbitas planetárias quanto nos auxilia na visão do inimaginavelmente pequeno das formas das moléculas.
Um excelente lembrete de que as disciplinas do conhecimento podem ser separadas para melhor administração de currículos escolares, mas que todas devem ser integradas na construção individual do conhecimento.
*Carlos Roberto de Lana é professor e engenheiro químico.
- Compostos Orgânicos: Características Gerais
Líria Alves A cetona é um composto orgânicoOs compostos orgânicos em sua maioria são formados pela ligação entre átomos de carbono e hidrogênio. Sendo assim, a atração entre elétrons das moléculas orgânicas é praticamente...
- Lei De Avogadro
Do número de Avogadro, sabemos que há aproximadamente 6,02 x 1023 átomos/mol. Então, em 0,0142 mol temos : (0,0142 mol) x (6,02 x 1023 átomos/mol) = 8,55 x 1021átomos Volume molar de um gás CNTP: temperatura = 0 °C e pressão =1atm. É o volume...
- Substâncias
Uma das maiores confusões que as pessoas fazem na hora de classificar as substâncias reside nos quesitos de substância simples e substância pura. Para que isso fique claro é fundamental que entendamos bem algumas coisas antes de chegarmos a essa...
- Química Geral
I - PROPRIEDADES DAS SUBSTÂNCIAS 1) Substância Iônica: Possuem elevados ponto de fusão (PF) e ponto de ebulição (PE);São solúveis em solventes polares;Conduzem a corrente elétrica quando fundidos (fase líquida) ou em solução aquosa, situações...
- A Ligação Covalente Da Quimica
Professor de Matemática e Biologia Antônio Carlos Carneiro BarrosoColégio Estadual Dinah Gonçalvesemail [email protected] www.ensinodematemtica.blogspot.com.brwww.accbarrosogestar.blogspot.com.br WWW.profantoniocarneiro.com ...
