Matemática
Hoje muito se fala da mecânica quântica. Conceitos como dualidade onda-partícula, sobreposição de estados ou influência do observador saíram da sala de aula e dos debates científicos para se tornarem assunto corrente até entre modalidades esotéricas. Não é difícil tal dispersão gerar confusão. O aluno interessado pode facilmente não entender.
O que, afinal de contas, princípios aparentemente tão complicados têm a ver com o aprendido sobre a estrutura dos átomos e o comportamento de suas partículas? Para ajudar esse aluno, existem os números quânticos, que identificam os elétrons a partir das características que lhes são atribuídas pela mecânica quântica.
Modelo atômico de Rutherford-Bohr
Para entendermos melhor os númeors quânticos, o melhor é começar por algo que todo mundo conhece: o modelo atômico de Rutherford-Bohr:
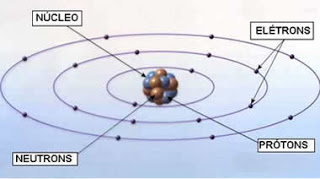
Neste modelo, o átomo é representado como um sistema solar. O núcleo ocupa o lugar do Sol, em torno do qual os elétrons descrevem órbitas circulares. Pode-se dizer que Rutherford e Bohr reproduziram o macrocosmo da física clássica newtoniana no microcosmo atômico.
A chegada da física quântica
As propriedades químicas dos elementos eram explicadas por sua distribuição eletrônica, o modo como os elétrons se distribuíam pelas órbitas ou camadas em torno do núcleo, normalmente identificadas pelas letras K, L, M, N, O, P e Q.
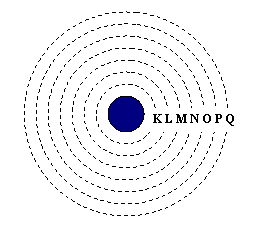
Figura 2: Distribuição eletrônica: camadas em torno do núcleo atômico
Quando as teorias quânticas conquistaram o reconhecimento dos físicos, era inevitável que a concepção do átomo como sistema planetário fosse revista, por ser incompatível com as descobertas naquele campo. Primeiro porque o elétron no modelo de Rutherford-Bohr era uma partícula, enquanto a mecânica quântica define o elétron pelo princípio da dualidade onda-partícula. Ou seja, ele pode ser tanto uma coisa quanto a outra. O Princípio da Incerteza de Heinsenberg afirma que além de o elétron não ser apenas uma partícula, seu comportamento não obedece ao determinismo da física clássica. Assim, não é possível precisar simultaneamente a velocidade e a posição de um elétron. Seu estudo só pode ser feito por uma abordagem probabilística.
Camadas: níveis de energia
O elétron não podia mais ser visto como uma partícula orbitando "classicamente" o núcleo, mas o modelo de distribuição eletrônica por camadas explicava tão bem o comportamento químico dos elementos que, do ponto de vista didático, podemos apenas adaptá-lo à nova concepção. Assim, essas camadas deixam de ser consideradas órbitas e passam a ser níveis de energia, diretamente relacionados com a distância média do elétron em relação ao núcleo. Quando substituímos as letras identificadoras das camadas por números, temos a seguinte correspondência, que define o primeiro dos números quânticos, chamado de Principal.
CAMADA
K
L
M
N
O
P
Q
1
2
3
4
5
6
7
NÍVEL
O número quântico principal expressa o nível de energia do elétron, definido por sua distância média do núcleo. O segundo número quântico é chamado de momento angular ou azimutal e define a forma dos orbitais dos elétrons.
Diferença entre órbita e orbital
Enquanto órbita indica uma trajetória regular do elétron em torno do núcleo, orbital indica uma região do espaço onde há grande probabilidade de encontrarmos um elétron. Didaticamente, é a tradução de um conceito clássico determinista para outro quântico e probabilístico. Os orbitais estão relacionados com subníveis de energia nos quais os elétrons se situam dentro do nível principal. Estes subníveis podem ser expressos pelo número quântico azimutal ou por letras convencionadas correspondentes, conforme abaixo:
SUBNÍVEL
s
p
d
f
NÚMERO QUÂNTICO AZIMUTAL
0
1
2
3
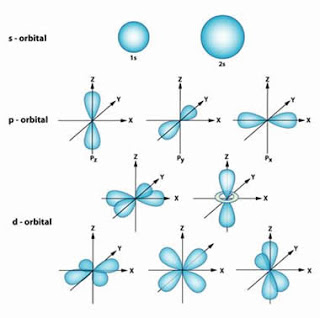
Figura 3: Formatos de orbitais de cada subnível
O número quântico magnético indica a orientação dos orbitais no espaço. Mostra como os orbitais se posicionam em relação ao seu eixo de coordenadas tridimensionais xyz, como ilustrado na figura 3. No caso do orbital d, temos cinco orientações possíveis para suas elipses, representadas pelos números quânticos magnéticos -2, -1, 0, 1 e 2. E, por último, o número quântico spin, que determina a rotação do elétron sobre seu próprio eixo, sendo cada sentido de giro identificado por -1/2 ou + 1/2.
Um primeiro passo
Os números quânticos originam-se de teorias complexas, desdobramentos da Equação de Schrödinger, que descreve analiticamente a função de onda do elétron. Talvez um primeiro contato com esses números deixe uma impressão algo nebulosa. Fazer a transição de conceitos do átomo sistema solar da figura 1 para os orbitais probabilísticos da figura 3 é um primeiro passo para entender os fundamentos da quântica por caminhos mais ortodoxos e seguros que os repassados nas versões esotéricas.
Carlos Roberto de Lana é engenheiro químico e professor.
- Princípio Da Incerteza
A "experiência de Young'' para elétrons, em particular a formação de uma figura de interferência mesmo quando o feixe de elétrons é tão rarefeito que não há dúvida de que os elétrons chegam um a um na tela, mostra que a física dos...
- Modelos Atômicos
O Modelo atômico de Dalton Vários pensadores propuseram que a matéria seria constituída por átomos, assim como havia pensado Demócrito e Leucipo. Todavia, até a primeira metade do século XIX, esse modelo ainda não era aceito pela comunidade científica....
- Modelo Atômico Atual: Distribuição Eletrônica
Modelo Atômico Atual: Distribuição EletrônicaA distribuição eletronica nos descreve o arranjo dos elétrons em um átomo, fornecendo o número de elétrons em cada nível principal e subnível. Os elétrons preenchem os subníveis em ordem crescente...
- Distribuição Eletrônica De Elétrons
Os elétrons estão distribuídos em camadas ao redor do núcleo. Admite-se a existência de 7 camadas eletrônicas, designados pelas letras maiúsculas: K,L,M,N,O,P e Q. À medida que as camadas se afastam do núcleo, aumenta a energia dos elétrons...
- Átomos
Há muito tempo, cerca de 30 anos antes de Cristo, o filósofo grego Demócrito já afirmava que a matéria era formada por partículas muito pequenas, às quais ele chamou de átomos. Entretanto o conceito de átomo desse filósofo é bem diferente do...
Matemática
Números quânticos Como encontrar e identificar o elétron
Professor de Matemática Antonio Carlos Carneiro Barroso
Colégio Estadual Dinah Gonçalves
email [email protected]
Blog HTTP://ensinodematemtica.blogspot.com
http://accbarrosogestar.blogspot.com.br
www.accbarrosogestar.wordpress.comHoje muito se fala da mecânica quântica. Conceitos como dualidade onda-partícula, sobreposição de estados ou influência do observador saíram da sala de aula e dos debates científicos para se tornarem assunto corrente até entre modalidades esotéricas. Não é difícil tal dispersão gerar confusão. O aluno interessado pode facilmente não entender.
O que, afinal de contas, princípios aparentemente tão complicados têm a ver com o aprendido sobre a estrutura dos átomos e o comportamento de suas partículas? Para ajudar esse aluno, existem os números quânticos, que identificam os elétrons a partir das características que lhes são atribuídas pela mecânica quântica.
Modelo atômico de Rutherford-Bohr
Para entendermos melhor os númeors quânticos, o melhor é começar por algo que todo mundo conhece: o modelo atômico de Rutherford-Bohr:

Neste modelo, o átomo é representado como um sistema solar. O núcleo ocupa o lugar do Sol, em torno do qual os elétrons descrevem órbitas circulares. Pode-se dizer que Rutherford e Bohr reproduziram o macrocosmo da física clássica newtoniana no microcosmo atômico.
A chegada da física quântica
As propriedades químicas dos elementos eram explicadas por sua distribuição eletrônica, o modo como os elétrons se distribuíam pelas órbitas ou camadas em torno do núcleo, normalmente identificadas pelas letras K, L, M, N, O, P e Q.

Figura 2: Distribuição eletrônica: camadas em torno do núcleo atômico
Quando as teorias quânticas conquistaram o reconhecimento dos físicos, era inevitável que a concepção do átomo como sistema planetário fosse revista, por ser incompatível com as descobertas naquele campo. Primeiro porque o elétron no modelo de Rutherford-Bohr era uma partícula, enquanto a mecânica quântica define o elétron pelo princípio da dualidade onda-partícula. Ou seja, ele pode ser tanto uma coisa quanto a outra. O Princípio da Incerteza de Heinsenberg afirma que além de o elétron não ser apenas uma partícula, seu comportamento não obedece ao determinismo da física clássica. Assim, não é possível precisar simultaneamente a velocidade e a posição de um elétron. Seu estudo só pode ser feito por uma abordagem probabilística.
Camadas: níveis de energia
O elétron não podia mais ser visto como uma partícula orbitando "classicamente" o núcleo, mas o modelo de distribuição eletrônica por camadas explicava tão bem o comportamento químico dos elementos que, do ponto de vista didático, podemos apenas adaptá-lo à nova concepção. Assim, essas camadas deixam de ser consideradas órbitas e passam a ser níveis de energia, diretamente relacionados com a distância média do elétron em relação ao núcleo. Quando substituímos as letras identificadoras das camadas por números, temos a seguinte correspondência, que define o primeiro dos números quânticos, chamado de Principal.
CAMADA
K
L
M
N
O
P
Q
1
2
3
4
5
6
7
NÍVEL
O número quântico principal expressa o nível de energia do elétron, definido por sua distância média do núcleo. O segundo número quântico é chamado de momento angular ou azimutal e define a forma dos orbitais dos elétrons.
Diferença entre órbita e orbital
Enquanto órbita indica uma trajetória regular do elétron em torno do núcleo, orbital indica uma região do espaço onde há grande probabilidade de encontrarmos um elétron. Didaticamente, é a tradução de um conceito clássico determinista para outro quântico e probabilístico. Os orbitais estão relacionados com subníveis de energia nos quais os elétrons se situam dentro do nível principal. Estes subníveis podem ser expressos pelo número quântico azimutal ou por letras convencionadas correspondentes, conforme abaixo:
SUBNÍVEL
s
p
d
f
NÚMERO QUÂNTICO AZIMUTAL
0
1
2
3

Figura 3: Formatos de orbitais de cada subnível
O número quântico magnético indica a orientação dos orbitais no espaço. Mostra como os orbitais se posicionam em relação ao seu eixo de coordenadas tridimensionais xyz, como ilustrado na figura 3. No caso do orbital d, temos cinco orientações possíveis para suas elipses, representadas pelos números quânticos magnéticos -2, -1, 0, 1 e 2. E, por último, o número quântico spin, que determina a rotação do elétron sobre seu próprio eixo, sendo cada sentido de giro identificado por -1/2 ou + 1/2.
Um primeiro passo
Os números quânticos originam-se de teorias complexas, desdobramentos da Equação de Schrödinger, que descreve analiticamente a função de onda do elétron. Talvez um primeiro contato com esses números deixe uma impressão algo nebulosa. Fazer a transição de conceitos do átomo sistema solar da figura 1 para os orbitais probabilísticos da figura 3 é um primeiro passo para entender os fundamentos da quântica por caminhos mais ortodoxos e seguros que os repassados nas versões esotéricas.
Carlos Roberto de Lana é engenheiro químico e professor.
- Princípio Da Incerteza
A "experiência de Young'' para elétrons, em particular a formação de uma figura de interferência mesmo quando o feixe de elétrons é tão rarefeito que não há dúvida de que os elétrons chegam um a um na tela, mostra que a física dos...
- Modelos Atômicos
O Modelo atômico de Dalton Vários pensadores propuseram que a matéria seria constituída por átomos, assim como havia pensado Demócrito e Leucipo. Todavia, até a primeira metade do século XIX, esse modelo ainda não era aceito pela comunidade científica....
- Modelo Atômico Atual: Distribuição Eletrônica
Modelo Atômico Atual: Distribuição EletrônicaA distribuição eletronica nos descreve o arranjo dos elétrons em um átomo, fornecendo o número de elétrons em cada nível principal e subnível. Os elétrons preenchem os subníveis em ordem crescente...
- Distribuição Eletrônica De Elétrons
Os elétrons estão distribuídos em camadas ao redor do núcleo. Admite-se a existência de 7 camadas eletrônicas, designados pelas letras maiúsculas: K,L,M,N,O,P e Q. À medida que as camadas se afastam do núcleo, aumenta a energia dos elétrons...
- Átomos
Há muito tempo, cerca de 30 anos antes de Cristo, o filósofo grego Demócrito já afirmava que a matéria era formada por partículas muito pequenas, às quais ele chamou de átomos. Entretanto o conceito de átomo desse filósofo é bem diferente do...
